CHIEF: Innovando la forma en que detectamos y diagnosticamos el cáncer.
- zoeziegler32
- hace 6 horas
- 7 Min. de lectura
Escrito por Zoe Ziegler
Fuentes enlazadas al final de la página
Última actualización: 3/6/26
Imagine que, tras esperar semanas por los resultados de su mamografía, le digan: «Usted no tiene cáncer de mama». Usted sigue con su vida. Meses después, regresa a la consulta del médico. Una exploración posterior revela la verdad: el cáncer había estado ahí todo el tiempo y había crecido. Oculto a plena vista y pasado por alto. Solo para descubrir más tarde que aquella primera prueba de detección podría haber marcado la diferencia entre un tratamiento temprano y un cáncer en una etapa avanzada. Si tan solo el médico lo hubiera visto. Es aquí donde la inteligencia artificial (IA) se está integrando en el diagnóstico por imagen mamario en hospitales reales, allanando el camino para que tecnologías como CHIEF mejoren la detección del cáncer.
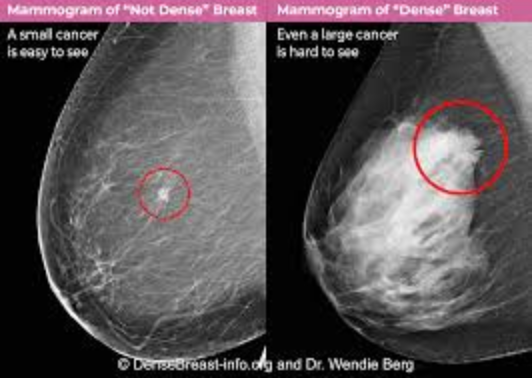
Un falso negativo es una realidad para muchas mujeres, y puede resultar devastador. Las mamografías de detección pueden pasar por alto aproximadamente 1 de cada 8 casos de cáncer de mama. De hecho, en un estudio, los investigadores identificaron 155 casos en los que el cáncer no fue detectado, ocurriendo esto con mayor frecuencia durante las mamografías de detección rutinarias. Aún más preocupante resulta el hecho de que muchas de estas pacientes contaban con antecedentes personales o familiares de cáncer de mama. Esto demuestra que los diagnósticos errados pueden ocurrir incluso cuando la paciente ya presenta un alto riesgo. Las tasas de cáncer no detectado pueden ser más elevadas en los casos de tejido mamario denso, ya que este enmascara los tumores, impidiendo que sean percibidos por el ojo humano.
Pero, ¿y si le dijera que existe una herramienta capaz de marcar la diferencia entre resultados prematuros y evitables, y transformar ese problema en detección temprana y atención personalizada —sin restar protagonismo a los profesionales de la salud, sino brindándoles un par de ojos adicional?
Los problemas de los fundamentos de la del pasado
Lo que estoy a punto de explicarle en el siguiente artículo no se limita simplemente al uso de sistemas de IA para realizar tareas que solo funcionan con tipos específicos de cáncer. Las bases de IA existentes —tanto las del pasado como las actuales— logran cierto éxito en la identificación del cáncer al analizar tejidos; sin embargo, investigadores de la revista *Nature* señalan que estas poseen una capacidad limitada —o incluso una total incapacidad— para funcionar eficazmente en situaciones nuevas.
Por ejemplo: supongamos que una IA ha sido entrenada en el Hospital A y ha estudiado las imágenes de diagnóstico generadas por los escáneres de dicho hospital. Aunque se trate de la misma enfermedad, si el Hospital A recibiera imágenes provenientes del Hospital B, la IA tendría dificultades para identificarlas debido a factores como la resolución, la iluminación, etc.
Del mismo modo, si dos sistemas de IA hubieran sido entrenados con datos demográficos de razas o grupos de edad distintos, es posible que su rendimiento no fuera el óptimo. Este constituye un problema fundamental en el ámbito de la IA médica.
En comparación con CHEIF, las bases de IA anteriores requerían múltiples sistemas independientes para realizar tareas diferentes; sería algo similar a tener una calculadora distinta para cada operación —suma, resta y multiplicación— en lugar de contar con una única calculadora capaz de realizar las tres. Precisamente por esta razón, CHEIF resulta tan innovador.
Por qué CHIEF es tan innovadora
"Nuestra ambición era crear una plataforma de IA ágil y versátil —similar a ChatGPT— capaz de realizar una amplia gama de tareas de evaluación oncológico", afirmó Kun-Hsing Yu, autor principal del estudio. Se proporcionaron a CHEIF 15 millones de imágenes; posteriormente, se le suministraron 60.000 imágenes de tejidos que incluían casos de cáncer de mama, así como de otros 20 tipos de cáncer. CHEIF alcanzó una precisión del 94 % en la detección del cáncer y superó a 15 conjuntos de datos correspondientes a enfoques actuales de IA. Asimismo, se recopilaron 32 conjuntos de datos independientes procedentes de 24 hospitales distintos, los cuales abarcaban una gran diversidad demográfica de personas de todo el mundo. Como ya mencioné, los sistemas de IA actuales carecen de fiabilidad, incluso al comparar los resultados entre diferentes hospitales.
¿Qué es un conjunto de datos?
ANALOGÍA: Un conjunto de datos consistiría en 10.000 imágenes de tumores cancerosos y 10.000 imágenes de tumores no cancerosos.
Y cada una de esas fotos está etiquetada —correcta o incorrectamente. Por lo tanto, la IA debe identificar los patrones a partir de los ejemplos y someterse a pruebas basadas en ellos.
Esto demuestra cómo estos diversos conjuntos de datos evidencian que CHEIF funciona de manera excepcional en múltiples entornos; es una solución versátil y una IA unificada, y no una simple calculadora de una sola función. CHEIF posee una capacidad de adaptación ante la diversidad muy superior a la de sus homólogos, lo cual resulta fundamental para que los sistemas de IA logren generalizar o, en otras palabras, puedan implementarse con mayor facilidad en distintos hospitales.
Lo que esto significa para la detección del cáncer de mama
Los tumores pequeños son más difíciles de detectar, pero pueden marcar la mayor diferencia cuando se identifican en una etapa temprana; de este modo, las mujeres ya no tendrán que lidiar con la falsa esperanza de estar libres de cáncer. Esto conlleva una reducción de las biopsias innecesarias, una menor ansiedad para las pacientes y una disminución de los costos sanitarios. CHIEF ha sido entrenado con múltiples conjuntos de datos independientes procedentes de docenas de hospitales de todo el mundo. Esto beneficiará directamente a las mujeres de color —y, en particular, a las mujeres negras—, quienes presentan un riesgo un 43 % mayor de padecer cáncer de mama. Este sistema es más adaptable y más fácil de generalizar que los modelos anteriores, lo que permite disipar una de las mayores inquietudes asociadas al uso de la inteligencia artificial en el ámbito de las imágenes médicas.
Sistemas clínicos de IA que apoyan a los radiólogos
La carga de trabajo de los radiólogos aumenta a un ritmo estimado del 10 al 12 % anual. Un estudio diseñado para determinar si la capacidad de los médicos para detectar el cáncer disminuye a medida que leen mamografías de forma consecutiva reveló un descenso en la atención y la precisión tras examinar 35 mamografías.
A pesar de este descenso, la precisión general en la detección del cáncer se mantuvo estable tanto en el grupo de control como en el experimental. El creciente volumen de casos subraya la importancia de tecnologías como CHIEF, que ayudan a reducir la carga de trabajo sin llegar a sustituir la pericia humana. Dado que algunos hospitales carecen incluso de radiólogos especializados, las herramientas de inteligencia artificial (IA) pueden servir de apoyo a las comunidades con menos recursos y que se encuentran desatendidas.
DeepHealth, otra organización propiedad de RadNet, busca mitigar el estrés que sufren los radiólogos. Su objetivo es implementar un sistema operativo impulsado por IA clínica que mejore la detección de enfermedades; este sistema ya se está utilizando en hospitales reales y ofrece información valiosa para la atención de los pacientes, entre otras funcionalidades.
SmartMammo, uno de los sistemas de IA de DeepHealth para la detección del cáncer de mama, ha recibido la aprobación de la FDA y ya puede utilizarse en determinados equipos de mamografía. Las plataformas de IA de RadNet procesan millones de mamografías cada año. Se ha demostrado que estos sistemas son plenamente integrables en la práctica clínica, y no meramente experimentales. Si bien aún no todos los hospitales los utilizan, una mayor concienciación podría propiciar una adopción más generalizada en todos los ámbitos, brindando apoyo a los radiólogos y permitiendo detectar el cáncer de mama de manera más temprana y precisa.

Planificación ética: ¿qué hay de la privacidad de los datos?
¿Representa la IA un riesgo ético? Pues bien, la Ley de IA de la Unión Europea clasifica la IA médica como de «alto riesgo» de forma automática. Esto no significa que el uso médico de la IA sea intrínsecamente de alto riesgo; más bien, para que pueda ser utilizada efectivamente en los hospitales, debe someterse a estrictos controles de transparencia, seguridad y supervisión antes de implementarse en la práctica clínica. Por lo tanto, si se lanzara una herramienta como CHIEF, esta sería examinada minuciosamente, regulada conforme a la normativa HIPAA y sometida a un seguimiento constante. «Un hospital descubrió que más del 40 % de sus departamentos utilizaban herramientas de IA no aprobadas para la documentación». La verdadera preocupación ética podría no residir en las herramientas reguladas —como CHIEF—, sino en los sistemas no aprobados que carecen de supervisión.
Entre las características clave de una IA ética en el ámbito sanitario se incluyen:
Gestión de datos conforme a la normativa HIPAA, con cifrado de extremo a extremo
Salvaguardas contra las «alucinaciones» (errores generativos) para prevenir la desinformación
Integración de datos en tiempo real para evitar respuestas obsoletas o inexactas
Ingeniería de *prompts* (instrucciones) dinámica que se adapta al contexto clínico
Arquitecturas RAG (Generación Aumentada por Recuperación) duales que validan cruzadamente los resultados
La inteligencia artificial debe servir de apoyo a los médicos, no de sustituto. Es posible desarrollar estos sistemas con responsabilidad y transparencia; las herramientas de IA como CHIEF tienen el potencial de innovar en la atención sanitaria, en lugar de amenazarla.
El proyecto Herscreen ofrece recursos adicionales relacionados con este tema.
Fuentes: Elmore, J. G., et al. (1998). Ten-year risk of false positive screening mammograms and clinical breast examinations. New England Journal of Medicine. https://pubmed.ncbi.nlm.nih.gov/9545356/
University of California - Davis Health. "Half of all women experience false positive mammograms after 10 years of annual screening." ScienceDaily. ScienceDaily, 25 March 2022. <www.sciencedaily.com/releases/2022/03/220325122711.htm>.
(Pesheva, 2024) https://news.harvard.edu/gazette/story/2024/09/new-ai-tool-can-diagnose-cancer-guide-treatment-predict-patient-survival/
Wang, X., Zhao, J., Marostica, E. et al. A pathology foundation model for cancer diagnosis and prognosis prediction. Nature 634, 970–978 (2024). https://doi.org/10.1038/s41586-024-07894-z
(Taylor-Phillips et al.)https://pmc.ncbi.nlm.nih.gov/articles/PMC6636274/
(Axente, 2023) https://deephealth.com/press-releases/radnet-unveils-deephealth-a-pioneering-ai-powered-health-informatics-portfolio/
Franklin, Jordan et al. “False negative breast cancers on imaging and associated risk factors: a single institution six-year analysis.” Breast cancer research and treatment vol. 205,3 (2024): 507-520. doi:10.1007/s10549-024-07259-0 https://pubmed.ncbi.nlm.nih.gov/38483757/
“Limitations of Mammograms.” American Cancer Society, https://www.cancer.org/cancer/types/breast-cancer/screening-tests-and-early-detection/mammograms/limitations-of-mammograms.html


Comentarios